你了解的罕见病“脊髓性肌萎缩症”
许多读者可能阅读过某知名微信公众号推送的一篇名为“100万换孩子多活1年,你换吗?”的文章,这是一位叫“小鱼儿妈妈”的母亲讲述自己宝宝从发现异常到确诊为“SMA”疾病、由恐慌迷茫到坚强面对的心路历程。另外在“SMA之家”、“美儿SMA关爱中心”等多个公益组织的网站上我们都能看到很多家庭与SMA抗争的故事,有痛苦也有挣扎。那么到底什么是SMA?为什么会患病?怎样避免患病?以及目前针对SMA的治疗药物有哪些?今天跟随我们来了解一下这一并不罕见的“罕见病”吧。
01 什么是SMA?
SMA脊髓性肌萎缩症(Spinal Muscular Atrophy)是一类由脊髓前角运动神经元变性导致的肌肉无力、肌肉萎缩的疾病,SMA对人全身上下的肌肉都会造成侵害。在常见的疾病类型中,患者腿部无力的情况通常较手臂更为严重,吞咽和呼吸功能也会受到影响。SMA患者的认知功能、感官系统不受影响。SMA侵害的对象不分男女和种族,它在新生儿中的发病率约1/6000-1/10000,人群携带率为1/72~1/47,具有种族差异。上海地区的人群携带率为1.9%,柳州地区为1.2%,其它地区和民族尚未见报道,估计大陆地区人群携带率为1/83~1/42。
02 SMA致病基因与发病机制
SMA是一种常染色体隐性疾病,主要与位于5号染色体上的两个高度同源的基因SMN1和SMN2相关,二者序列同源性>99%,仅存在5个碱基差异,其中在第7外显子上的c.840的碱基差异(SMN1为C、SMN2为T)导致90%的SMN2 mRNA外显子7被选择性剪接,仅有10%的SMN2表达全长有功能SMN蛋白,SMN1可表达稳定完整功能的SMN蛋白,所以SMN1决定疾病的发生,SMN2只是影响疾病的严重程度及发病时间。
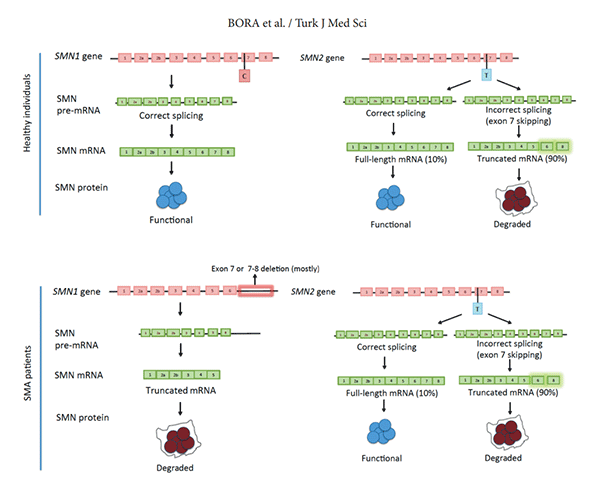
图1 SMN1、SMN2基因及功能示意图
03 SMA分型及临床
中国88%~95%的SMA患者是由SMN1基因7号外显子纯合缺失所致,其中大部分同时合并第8外显子的缺失。极少部分为SMN1基因第7外显子杂合缺失合并SMN1基因杂合性点突变或其他变异所致。
SMA根据发病时间和临床表现可分为Ⅰ~Ⅳ型(如表1)。SMA为婴幼儿中第二常见的致死性常染色体隐性遗传病。
表1 不同类型的SMA的临床特点
| 类型 | 发病年龄 | 生存期 | 最大运动能力 | 其他表现 |
| Ⅰ | <6个月 | ≤2岁(可能更久) | 无法独坐 | 轻度关节痉挛,吸吮/吞咽困难,舌肌震颤 |
| Ⅱ | 6~18个月 | 多数可达25岁 | 独坐 | 手指姿势性震颤 |
| Ⅲ | >18个月 | 正常 | 独立行走 | 无 |
| Ⅳ | 成年期 | 正常 | 正常 | 无 |
04 SMA与遗传
超过98%的SMA患儿,其父母都是携带者,其中95.5%的患者父母均为SMN1基因1拷贝杂合突变(1+0)的携带者;约4%为SMN1基因2拷贝杂合突变(2+0)的携带者,1~2%为生殖腺嵌合,抑或患者的突变属于新发突变(de novo)。因此,对于患儿的父母,无论其外周血基因检测结果是否提示为携带者,再次生育时均应进行产前诊断。
而对于正常的夫妻,由于SMA的人群携带率高1/83~1/42,对于未生育过SMA患者,但希望评估生育SMA患儿风险的夫妇,建议在充分知情同意的前提下,进行SMN1基因的携带者检测,若提示双方均携带SMN1基因杂合突变,则应为其提供产前或胚胎植入前诊断。
目前这一筛查策略已逐步达成共识。2017年,美国ACOG推荐备育或已育女性全部进行SMA筛查;2018年2月8日, 美国联邦咨询委员会建议所有新生儿进行SMA筛查。
05 SMA患者的治疗与管理
目前SMA的基因治疗药物,经FDA(Food and Drug Administration,美国食品药品监督管理局)上市批准的药物已有三种,分别为:Zolgensma, Nusinersen(诺西那生钠)和Nusinersen(司利扑兰)。
Nusinersen (Spinraza)由美国渤健公司推出,2016年12月通过FDA审批,是FDA批准上市的第一个治疗SMA 的药物,2019年4月28日,诺西那生钠注射液在中国上市。曾因“70万元一针”在我国引发热议,但在近日得到了纳入医保的好消息,并于2022年1月1日起正式开始执行。该药物需要鞘内注射,第一个月每两周注射一次,之后每30天注射一次,再随后每4个月注射1次,并持续终生。
Risdiplam(Evrysdi)由罗氏、PTC治疗公司和SMA基金会联合开发,用于治疗2个月以上SMA患者。是一种高效的SMN2小分子剪接修饰剂。它于2020年8月获得FDA批准,2021年6月,司利扑兰获得中国国家药监局批准上市。
Zolgensma (Onasemnogene adeparvovec-xioi)由AveXis,Inc.开发,2018年诺华公司收购AveXis,Inc.,2019年5月该药获FDA批准,给药方式为静脉一次注射。
后两种药物目前暂未纳入医保,治疗费用高昂。
06 SMA与基因检测方案
上文提到95%以上的SMA患者都会检测到SMN1基因外显子7和(或)外显子8纯合缺失,分子诊断的方法包括PCR-限制性片段长度多态性(PCR-RFLP)、实时荧光定量PCR(real-time PCR)、多种连接探针扩增(multiple ligation-dependent probe amplification, MLPA)等方法进行。
其中real-time PCR主要检测SMN1基因常见突变即第7和第8外显子的缺失突变,可以快速、经济地筛查人群中的携带者。MLPA的方法,除了检测常见外显子的缺失外,还针对SMN1基因内部分常见点突变设计探针进行检测,周期稍长,价格更高,更适合对临床疑似患儿的分子诊断,对于只检出SMN1基因第7外显子杂合缺失者,还可以补充SMN1基因的测序测定。
上一篇: 抗缪勒管激素与生殖内分泌


























